1.
Transferencia de masa
Evidentemente, la frontera que demarca la actividad aeróbica y anaeróbica depende de la concentración de oxígeno local en el seno del fluido, del coeficiente de difusión de oxígeno y de las velocidades de respiración locales en la región aeróbica. En los procesos aeróbicos la aireación adecuada es lo más importante. La demanda de oxígeno, que depende del tipo de sustrato utilizado y de las células involucradas en el proceso, se puede calcular con base en la siguiente ecuación
1. |
Donde, C es la demanda de oxígeno de la masa de células formada; A es la cantidad de oxígeno necesaria para la oxidación del sustrato a dióxido de carbono y agua; B es la cantidad de oxígeno necesaria para la oxidación de la masa celular a dióxido de carbono y agua, Y es el coeficiente de rendimiento de biomasa en sustrato (YX/S) o en oxígeno (YX/O).
La solubilidad del oxígeno en soluciones acuosas a 1 atmósfera de presión y temperatura cercana a la ambiental, es del orden de 10 ppm. Una población de levaduras con respiración activa puede consumir oxígeno a una velocidad de 0,3 g de oxígeno por hora y por gramo de células secas. El valor máximo de consumo de oxígeno para una población con densidad de 109 células por mililitro, se estima con la suposición que el volumen celular es de 10-10 mililitros, del cual el 80% es agua. La demanda absoluta de oxígeno es
= 6.10-3 g/(ml h) = 6 g O2/(l h)
De esta forma, la población con respiración activa consume oxígeno a una velocidad que es aproximadamente 750 veces mayor al valor de saturación de O2 por hora. Como la cantidad de gas disuelto es relativamente pequeña, se debe añadir gas continuamente al líquido con el fin de mantener viable la población celular. Esto no es una tarea fácil, puesto que la baja solubilidad del oxígeno ocasiona que la diferencia de concentración que conduce la transferencia de oxígeno de una zona a otra, siempre sea muy pequeña.
La demanda específica de oxígeno por gramo de biomasa presente, es producto de la demanda absoluta y de la velocidad de crecimiento. Por ejemplo, la producción de ácido glucónico con Pseudomonas ovalis requiere 620 ml de oxígeno por litro y por hora; así mismo, la producción de ácido acético con Acetobacter suboxydans necesita 500 ml de oxígeno por litro y por hora.
La velocidad de consumo de oxígeno está controlada por las velocidades de transferencia a través de las películas que se forman alrededor de las burbujas de gas y de las células y por la resistencia a la transferencia de masa a través de la masa de fluido (ver figura 1). La película de líquido alrededor de la burbuja de gas representa la mayor resistencia a la transferencia para gases muy poco solubles.
Figura 1. Transporte de oxígeno desde una burbuja de gas hasta una célula
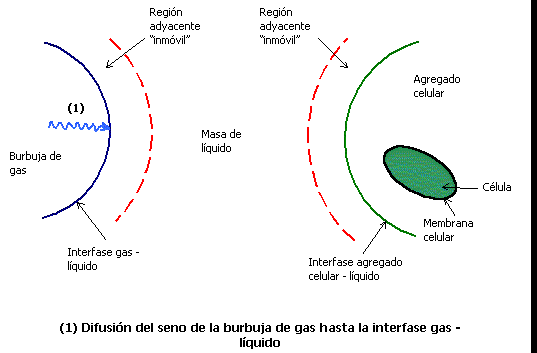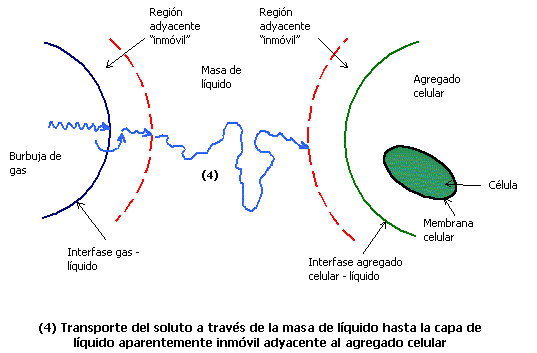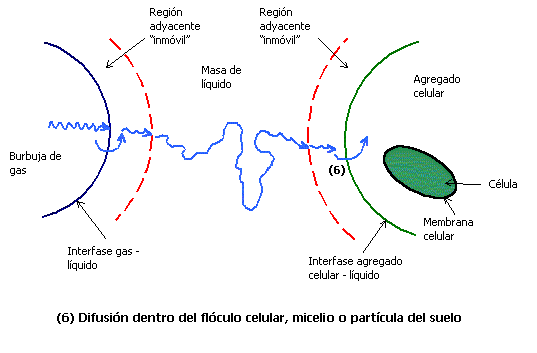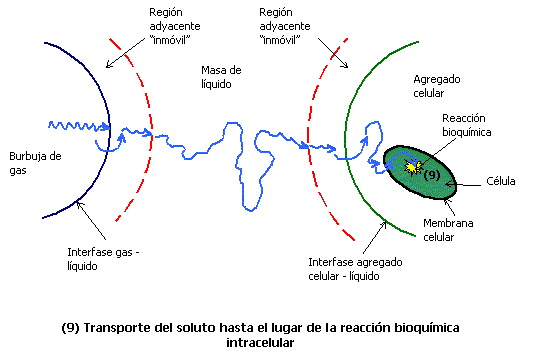
Para especies muy poco solubles en agua, tales como oxígeno o hidrocarburos, las dos concentraciones interfaciales de equilibrio cgi y cli del lado del gas y del líquido respectivamente, pueden relacionarse por medio de una ley lineal de partición como la ley de Henry
2. |
que estipula que la velocidad de intercambio de soluto a través de la interfase es mucho mayor que la velocidad de transferencia neta, como en este caso: a 1 atmósfera de presión y 25ºC, la velocidad de colisión de O2 en la superficie es del orden de 1024 moléculas por centímetro cuadrado y por segundo, un valor muy por encima del flujo neto para los requerimientos típicos de consumo microbial mencionados anteriormente.
En estado estable, la velocidad de transferencia de oxígeno a la interfase gas – líquido es igual a la velocidad de transferencia de oxígeno a través de la película del lado del líquido (figura 1). Si se toman cg y cl como las concentraciones de oxígeno en el seno del gas y en el seno del líquido respectivamente, se puede escribir
| Flujo (flux) de oxígeno | = [mol O2/(cm2 s)] | |
3. |
||
4. |
Como las concentraciones interfaciales generalmente no pueden medirse, las ecuaciones de transferencia se expresan en función del coeficiente global de transferencia de masa Kl y de la concentración global o fuerza conductora c*l – cl, donde c*l es la concentración en la fase líquida la cual está en equilibrio con la fase gaseosa
5. |
Con base en estas cantidades globales, el flujo (flux) de soluto está dado por
6. |
De las ecuaciones 2 a 6, se obtiene la conocida relación entre el coeficiente global de transferencia de masa Kl y los parámetros físicos del problema de transporte de la doble película, kg, kl y M
7. |
Para las especies poco solubles, M es mucho mayor que la unidad. Además, kg es considerablemente mayor que kl. En estas circunstancias, se observa con base en la ecuación 7 que Kl es aproximadamente igual a kl. Por lo anterior, toda la resistencia a la transferencia de masa reside, esencialmente, del lado del líquido.
La velocidad de transferencia de oxígeno por unidad de volumen de líquido (VTO), está dada por:
VTO = velocidad de absorción de oxígeno =
[(flux) (área interfacial)]/volumen de líquido en el reactor
8. |
Donde, kla es el coeficiente volumétrico de transferencia de masa; a = A/V es el área interfacial gas – líquido por unidad de volumen, y se utiliza la aproximación Kl » kl descrita anteriormente.
Es importante reconocer que
VTO se define "en el punto". Ésta es una velocidad
volumétrica local de consumo de oxígeno; la velocidad
volumétrica promedio de utilización de oxígeno (moles por
tiempo por unidad de volumen) ![]() , en la totalidad del volumen de líquido V es
, en la totalidad del volumen de líquido V es
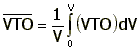 |
9. |
En general ![]() es igual a VTO, únicamente si las
condiciones hidrodinámicas, la relación entre el área
interfacial y el volumen, y las concentraciones de oxígeno son
uniformes a lo largo del reactor.
es igual a VTO, únicamente si las
condiciones hidrodinámicas, la relación entre el área
interfacial y el volumen, y las concentraciones de oxígeno son
uniformes a lo largo del reactor.
Teóricamente, la velocidad de demanda de oxígeno es máxima cuando la concentración de oxígeno disuelto en el líquido se aproxima a cero. Sin embargo, con el fin de mantener el sistema activo, tiene que mantenerse una concentración crítica mínima de oxígeno disuelto, cl,crit, por encima de la cual no hay un aumento apreciable de la demanda de oxígeno. La tabla 1 presenta algunos ejemplos de los niveles críticos de oxígeno para algunos microorganismos. Si cl = cl,crit el suministro de oxígeno será óptimo y la agitación del sistema la más apropiada.
Tabla 1.
| Organismo | Temperatura (ºC) | cl, crit (mmol O2/l) |
| Azotobacter vinelandii | 30 | 0,018 – 0,049 |
| E. coli | 37,8 | 0,0082 |
| 15 | 0,0031 | |
| Serratia marcescens | 31 | ~ 0,015 |
| Pseudomonas denitrificans | 30 | ~ 0,009 |
| Levadura | 34,8 | 0,0046 |
| 20 | 0,0037 | |
| Penicillium chrysogenum | 24 | ~ 0,022 |
| 30 | ~ 0,009 | |
| Aspergillus oryzae | 30 | ~ 0,020 |