1.
Inactivación (desnaturalización) de enzimas
La mayor parte de la literatura sobre cinética de enzimas se dedica a la información sobre la velocidad inicial de reacción y el análisis de la actividad enzimática. Sin embargo, en algunas aplicaciones y configuraciones de proceso, una propiedad crítica es la velocidad a la cual la actividad enzimática declina. Esto es especialmente cierto cuando se considera el uso de enzimas a gran escala en un reactor de flujo continuo.
Las enzimas se pueden inactivar (desnaturalizar) principalmente por envenenamiento, contaminación microbial, sedimentación y desnaturalización química. Esta pérdida de actividad se describe frecuentemente por la ecuación de velocidad de primer orden
1. |
Donde cE es la concentración de la enzima y kd la constante de inactivación.
La relación entre la actividad enzimática y la temperatura tiene un máximo debido a los efectos de la desnaturalización. Puede asumirse un equilibrio entre la enzima activa y la enzima desnaturalizada (inactiva)
2. |
Con constante de equilibrio
3. |
Con base en las ecuaciones anteriores se tiene que
4. |
Donde, cE0 es la concentración inicial de enzima. La velocidad máxima de reacción del complejo activado está dada por
5. |
Donde D HA es la entalpía de activación. La constante de equilibrio esta dada por
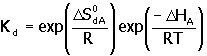 |
6. |
Donde D S0d es la entropía de inactivación. Las ecuaciones 4 a 6 proveen la siguiente relación entre la máxima velocidad de reacción rmax con la temperatura:
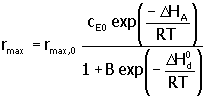 |
7. |
Esta ecuación describe el pico máximo de temperatura observado en todas las reacciones con enzimas.