1.
Modelo de Briggs – Haldane
El modelo propuesto por Briggs y Haldane (1925), aplicable al complejo intermedio, ES, es válido para reacciones en un sistema cerrado, siempre que cS0 >> cE0. La reacción S -k® P, no alcanza el equilibrio si la velocidad de descomposición del complejo ES, hasta producto y enzima libre, es rápida, comparada con la velocidad de disociación de ES, hasta E + S.
En un sistema con una concentración inicial de sustrato mucho mayor que la concentración inicial de enzima, puede aplicarse la aproximación de estado cuasi – estable, d(cES)/dt = 0, al complejo intermedio.
Las ecuaciones de balance de masa, aplicables al sustrato S y al complejo ES, en el modelo propuesto por Briggs y Haldane son:
1. |
2. |
Las ecuaciones anteriores son ecuaciones diferenciales simultáneas y ordinarias con dos incógnitas cE y cES. Las condiciones iniciales apropiadas para resolver el sistema son: t = 0; cS = cS0; cES = 0.
Estas ecuaciones no pueden resolverse analíticamente, pero con la ayuda de un computador es posible calcular las concentraciones de E, S, ES y P, como funciones del tiempo.
En una célula viva las concentraciones de sustrato y de enzima son del mismo orden, y no se aplica la aproximación de estado cuasi – estable. Si en la ecuación 2. se reemplaza d(cES)/dt = 0, y se eliminan cE y cS mediante la ecuación cE0 = cE +(cES), se obtiene (Bailey y Ollis, 1986):
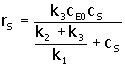 |
3. |
Puesto que, VM = k3cE0 ; KM, la constante de Michaelis, es:
4. |
Donde kS es la constante de disociación del complejo enzima – sustrato.
En la deducción de la ecuación de Michaelis – Menten, la constante de Michaelis, KM. es igual a la constante de disociación, KM = kS = k2/k1, mientras que en la deducción de la ecuación de Briggs – Haldane, KM = (k2 + k3)/k1. Estos valores de KM coinciden si k2 >> k3, lo cual significa que la etapa de liberación de producto es más lenta que la etapa de disociación del complejo enzima – sustrato.
Si se reemplazan k3cE0 y KM en la ecuación 3 se obtiene la ecuación de Michaelis – Menten, cuando esta ecuación se integra entre (t = 0; cS = cS0) y (t = t; cS = cS), se obtiene:
5. |
Donde t es el tiempo requerido para alcanzar una concentración determinada de sustrato.